在全球医药市场中,制定科学、高效的全球注册战略对于药品的成功开发、审批及上市至关重要。百联达凭借深厚的国际法规经验和跨国注册实战经验,为制药企业提供全生命周期的注册战略支持,确保产品高效合规进入全球市场,并保持长期竞争优势。
我们围绕药品生命周期的不同阶段,提供定制化的全球注册战略服务,包括:
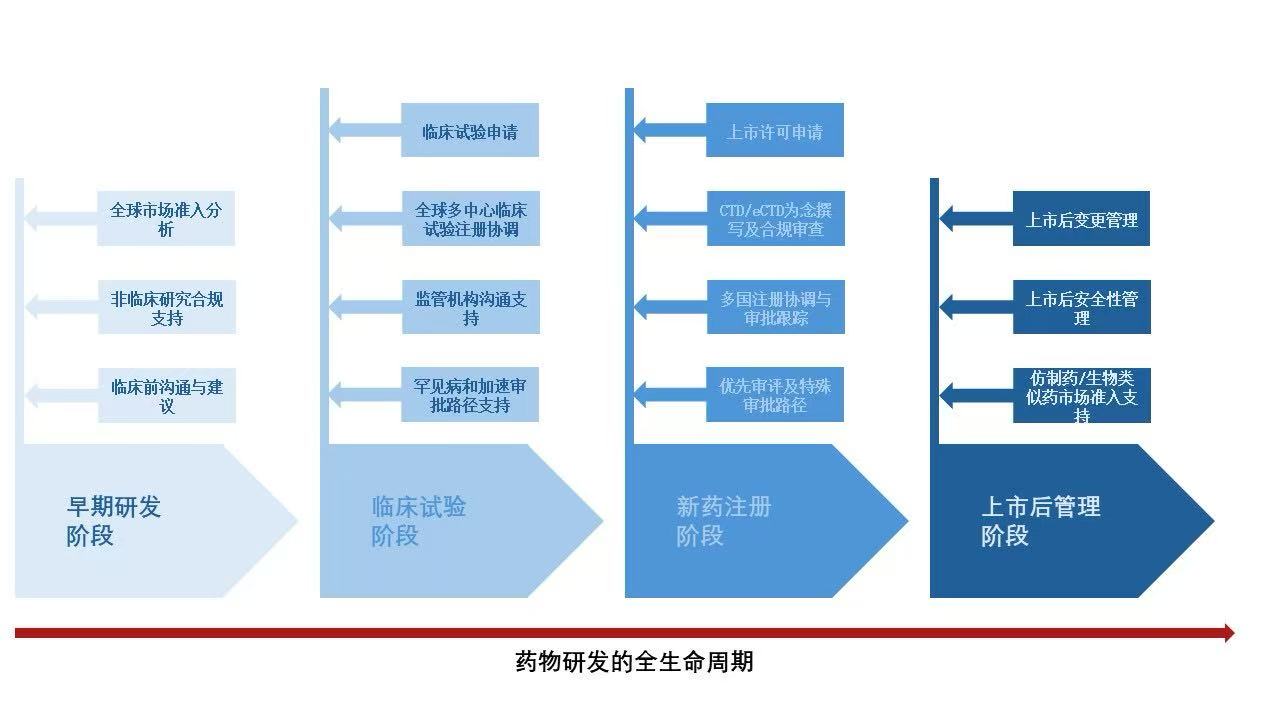
1. 早期研发阶段
在药品研发的早期阶段,制定正确的全球注册战略至关重要,我们提供:
· 全球市场准入分析:评估目标市场(如美国FDA、欧洲EMA、中国NMPA、新加坡HSA等)的法规要求,制定适合的注册策略。
· 非临床研究合规支持:指导企业符合GLP(良好实验室规范)要求,确保非临床研究数据符合国际标准。
· 临床前沟通与建议:协助企业与监管机构(如FDA Pre-IND、EMA Scientific Advice、NMPA CDE沟通会)进行早期交流,优化注册策略。
2. 临床试验阶段
临床试验的设计和注册策略直接影响药品的上市进度,我们提供:
· 临床试验申请(CTA/IND 申报):支持新药临床试验申请(IND)及临床试验许可(CTA)文件准备、提交及全生命周期管理。
· 全球多中心临床试验注册协调:确保临床试验符合各国法规要求,提高数据的全球适用性。
· 监管机构沟通支持:提供监管审评问询(Review Questions)应对策略,确保临床开发顺利推进。
· 罕见病和加速审批路径支持:指导企业申请孤儿药(Orphan Drug)、突破性疗法(Breakthrough Therapy)、快速通道(Fast Track)等特别通道,提高临床开发效率。
3. 新药注册阶段
成功的新药上市注册策略决定药品能否快速进入市场,我们提供:
· 上市许可申请(MAA/NDA/BLA):支持新药申请(NDA/BLA)及上市许可申请(MAA)的文件编制、审查和提交。
· CTD/eCTD 文件撰写及合规检查:确保注册申报文件符合 ICH CTD 结构及各国法规要求,提高审批成功率。
· 多国注册协调与审批跟踪:确保药品同步在多个国家和地区提交注册申请,提高全球市场覆盖率。
· 优先审评及特殊审批路径:支持快速审批(Priority Review)、条件批准(Conditional Approval)等政策申请,加速产品上市。
4. 上市后管理阶段(Post-Marketing & Lifecycle Management)
药品成功上市后仍需持续的合规管理及注册维护,我们提供:
· 上市后变更管理(Variation & Lifecycle Management):支持CMC变更、新增适应症、剂型优化、生产变更等监管事务。
· 上市后安全性管理(Pharmacovigilance):确保符合各国药物警戒(PV)法规,支持上市后不良反应(ADR)监测和报告。
· 仿制药/生物类似药市场准入支持:为仿制药(ANDA)和生物类似药(Biosimilar)提供注册策略和市场准入支持,确保产品竞争优势。
展望未来,我们将继续加强技术创新和服务升级,推动制药行业的健康发展,为客户创造更大的价值。我们期待与全球客户合作,共创辉煌。
 北京市北京经济技术开发区广德大街20号院(中科电商谷)8号楼508室
北京市北京经济技术开发区广德大街20号院(中科电商谷)8号楼508室
 +86 15010496015
+86 15010496015
 Admin@brilliantmed.cn
Admin@brilliantmed.cn